メソッド開発とカラム選択:FluoroPhenyl 固定相はどのようにHILIC・逆相の両モードで作用するのか
概要
難しい分離がうまくいくかどうかはカラムの保持と選択性によって大きく左右されるため、カラム選択はメソッド開発において重要です。一般的にはC18カラムが使用されますが、FluoroPhenylカラムはメソッド開発に全く異なる選択性をもたらします。これは、FluoroPhenylに複数の保持機構が組み込まれており、逆相モードと親水性相互作用クロマトグラフィー(HILIC)モードの両方で利用できるためです。ここでは、塩基性化合物や低分子極性化合物のように特にC18で分離が難しい化合物に対して、FluoroPhenylがどのように分離を改善するのかをご紹介します。
はじめに
C18固定相はこれまで多くのラボでLCカラムの主役を担ってきましたが、保持と選択性が限られているため、親水性化合物にとっては必ずしも最良の選択とはいえません。C18カラムは、主に分散力によって化合物を分離し、疎水性の保持をもたらすアルキル固定相を有します。この単一の保持機構は多くの逆相分析の基礎となっていますが、最終的にはC18の用途を、疎水性に基づいて分離しうる非極性な分析対象化合物に制限してしまいます。対照的に、RestekのFluoroPhenyl固定相では、分散、立体選択性、陽イオン交換、双極子、およびπ-π相互作用を含む複数の保持機構が作用します。この複合的な保持機構の存在がFluoroPhenylにC18の代わりとなる、もしくは全く異なる選択性をもたらし、低分子極性化合物や塩基性化合物を含む分離の難しい化合物に対する強力なツールとなります。FluoroPhenylは、フェニル基に電気陰性度の大きいフッ素原子を組み合わせることで、独自の選択性を実現しています(図1)。この固定相構造により、HILICと逆相の両モードを使用できるミックスモードカラムの機能が生じ、メソッド開発の際に分析対象成分に最善な分離モードを選ぶという自由度が得られます。ここでは、メソッド開発とカラム選択を検討し、C18と比較してFluoroPhenylで達成できるより広範囲な分離について示します。また、移動相の組成、酸強度や酸濃度などのパラメータを変更することで、どのように分離をコントロールし最適化するかについても触れます。
図 1: Raptor FluoroPhenyl LCカラムの仕様
| 固定相カテゴリ: | Pentafluorophenyl propyl (L43) |
| 官能基タイプ |
FluoroPhenyl |
| 粒子: |
2.7 µm or 5 µm superficially |
| 細孔径: |
90 Å |
| 表面積: |
150 m2/g (2.7 µm) |
| 推奨使用条件: |
pH Range: 2.0–8.0 |
複数の保持機構がC18に代わる選択性をFluoroPhenylカラムへもたらします
効率的かつ効果的なメソッド開発は、カラム選択にかかっています。 分析対象成分に最適なカラムを早い段階で選定することで、新しいメソッド開発に要する時間を節約できます。C18と比較した場合のFluoroPhenylの異なる選択性は、1本のカラムで複合的な保持機構を利用でき、メソッド開発担当者をサポートします。FluoroPhenyの独特の保持特性を解説し、HILICおよび逆相モードの両方についての性能を調べるために、いくつか分離が難しい化合物(図2)を選定しました。これらの化合物は全て従来のC18固定相では保持が弱いか分離が悪い、またはその両方であるためです。
図 2: Raptor FluoroPhenylカラムの複合的な保持モードを実証するために用いたテスト化合物
逆相モードにおける Vitamin D 異性体の立体選択性による保持
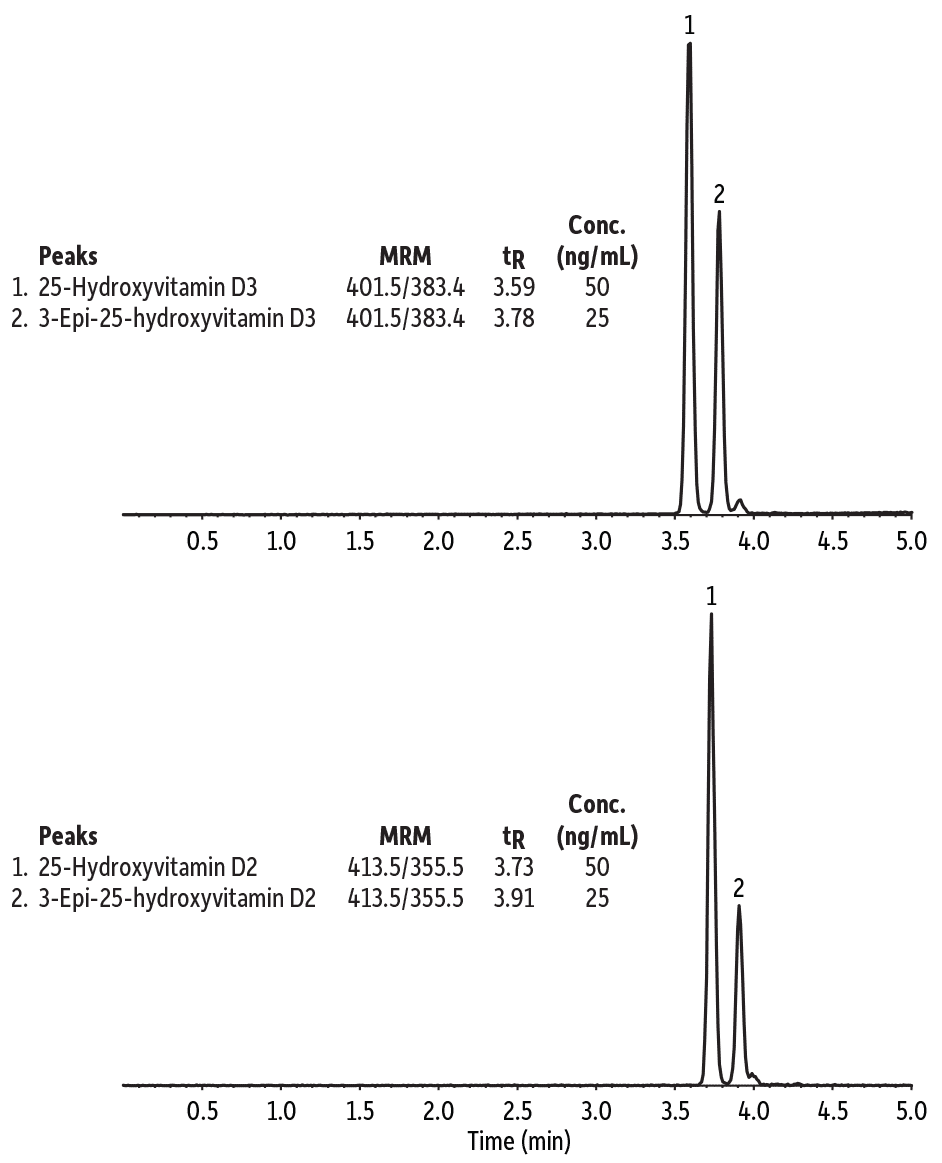
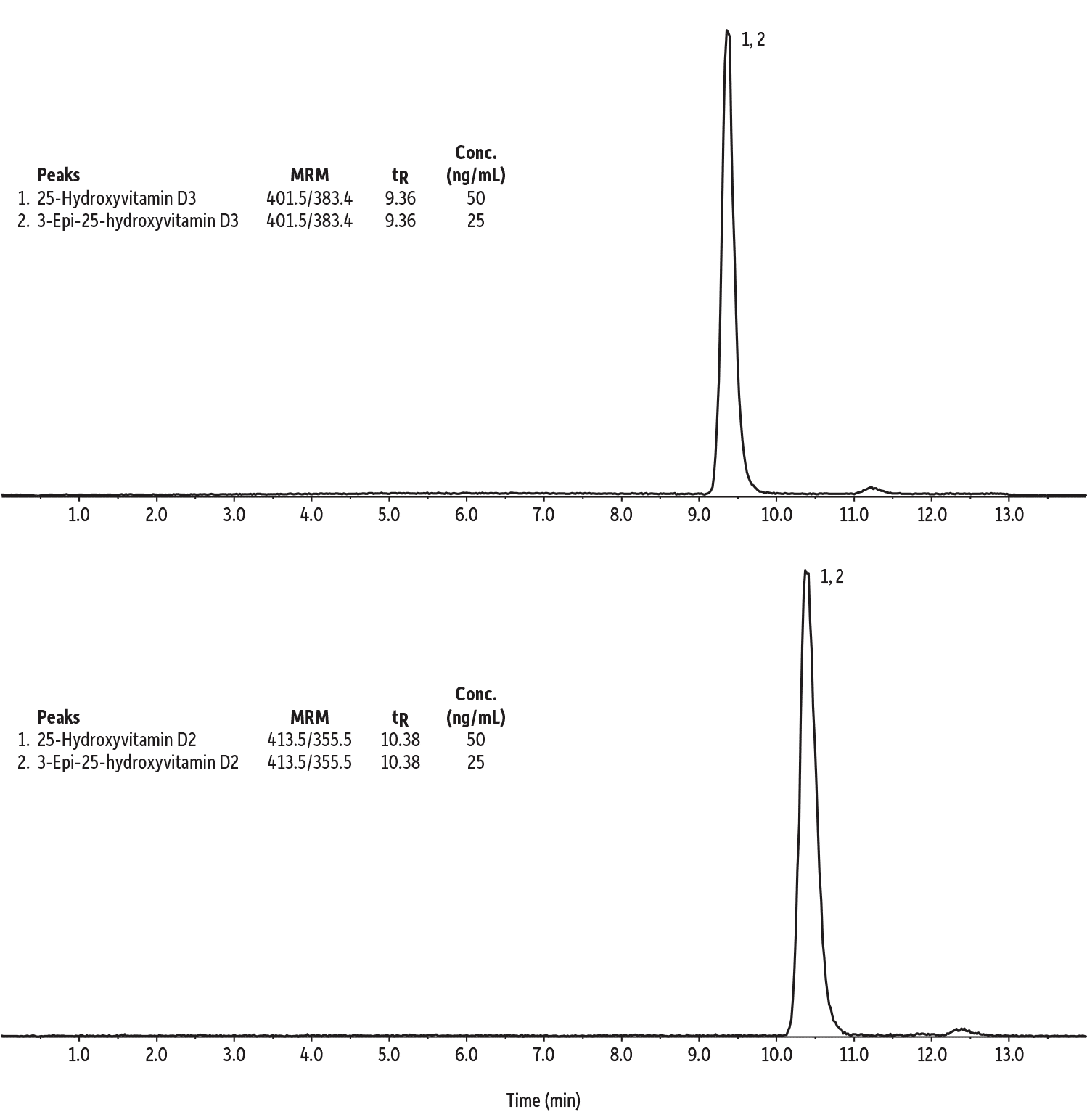
最初の例として、25-Hydroxyvitamin D3 とその C3エピマーの分析について評価を行いました。 この分離は世界中の臨床検査ラボで関心が高まっています。 25-Hydroxyvitamin D3は、ビタミンD代謝異常の判定に用いられる重要なバイオマーカーです。 C3エピマー (3-epi-25-hydroxyvitamin D3) は、生理活性がはるかに低いため、個々に測定しなければバイオマーカー値を過大評価する原因となります。 これらの化合物はアイソバリックであるため、クロマトグラフィー分離は正確な生体中濃度測定に不可欠です。 図3に示すように、逆相モードでFluoroPhenylを用いた場合、わずか5分で 25-Hydroxyvitamin D3とその C3エピマーを完全分離することができます。対照的に、C18カラムは溶出時間が3倍もかかっても、十分な分離は得られませんでした。この例において、カラム選択は、メソッド開発において明らかに重要な役割を果たしています。つまり、FluoroPhenylの立体的に安定な(リジットな)構造は、C18カラムの疎水性保持で得られるよりも、立体選択性を増し、本質的により多くの分離能が得られる結果となりました。
図 3: 立体選択的な保持力で C3エピマーと生理活性型を分離するため、FluoroPhenylを用いたVitamin D分析はより正確です。
Raptor FluoroPhenyl
| Column | Raptor FluoroPhenyl (cat.# 9319A1E) | ||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Dimensions: | 100 mm x 3 mm ID | ||||||||||||||||||||||||||||
| Particle Size: | 2.7 µm | ||||||||||||||||||||||||||||
| Temp.: | 30 °C | ||||||||||||||||||||||||||||
| Standard/Sample | |||||||||||||||||||||||||||||
| Diluent: | Water:methanol (50:50) | ||||||||||||||||||||||||||||
| Conc.: | 25-50 ng/mL | ||||||||||||||||||||||||||||
| Inj. Vol.: | 5 µL | ||||||||||||||||||||||||||||
| Mobile Phase | |||||||||||||||||||||||||||||
| A: | 0.1% Formic acid in water | ||||||||||||||||||||||||||||
| B: | Methanol | ||||||||||||||||||||||||||||
|
| Detector | MS/MS |
|---|---|
| Ion Mode: | ESI+ |
| Mode: | MRM |
| Instrument | HPLC |
Raptor ARC-18
| Column | Raptor ARC-18 (cat.# 9314A12) | ||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Dimensions: | 100 mm x 2.1 mm ID | ||||||||||||||||||||||||
| Particle Size: | 2.7 µm | ||||||||||||||||||||||||
| Temp.: | 30 °C | ||||||||||||||||||||||||
| Standard/Sample | |||||||||||||||||||||||||
| Diluent: | Water:methanol (50:50) | ||||||||||||||||||||||||
| Conc.: | 25-50 ng/mL | ||||||||||||||||||||||||
| Inj. Vol.: | 5 µL | ||||||||||||||||||||||||
| Mobile Phase | |||||||||||||||||||||||||
| A: | 0.1% Formic acid in water | ||||||||||||||||||||||||
| B: | Methanol | ||||||||||||||||||||||||
|
| Detector | MS/MS |
|---|---|
| Ion Mode: | ESI+ |
| Mode: | MRM |
| Instrument | HPLC |
HILICモードにおける低分子極性化合物の陽イオン交換作用
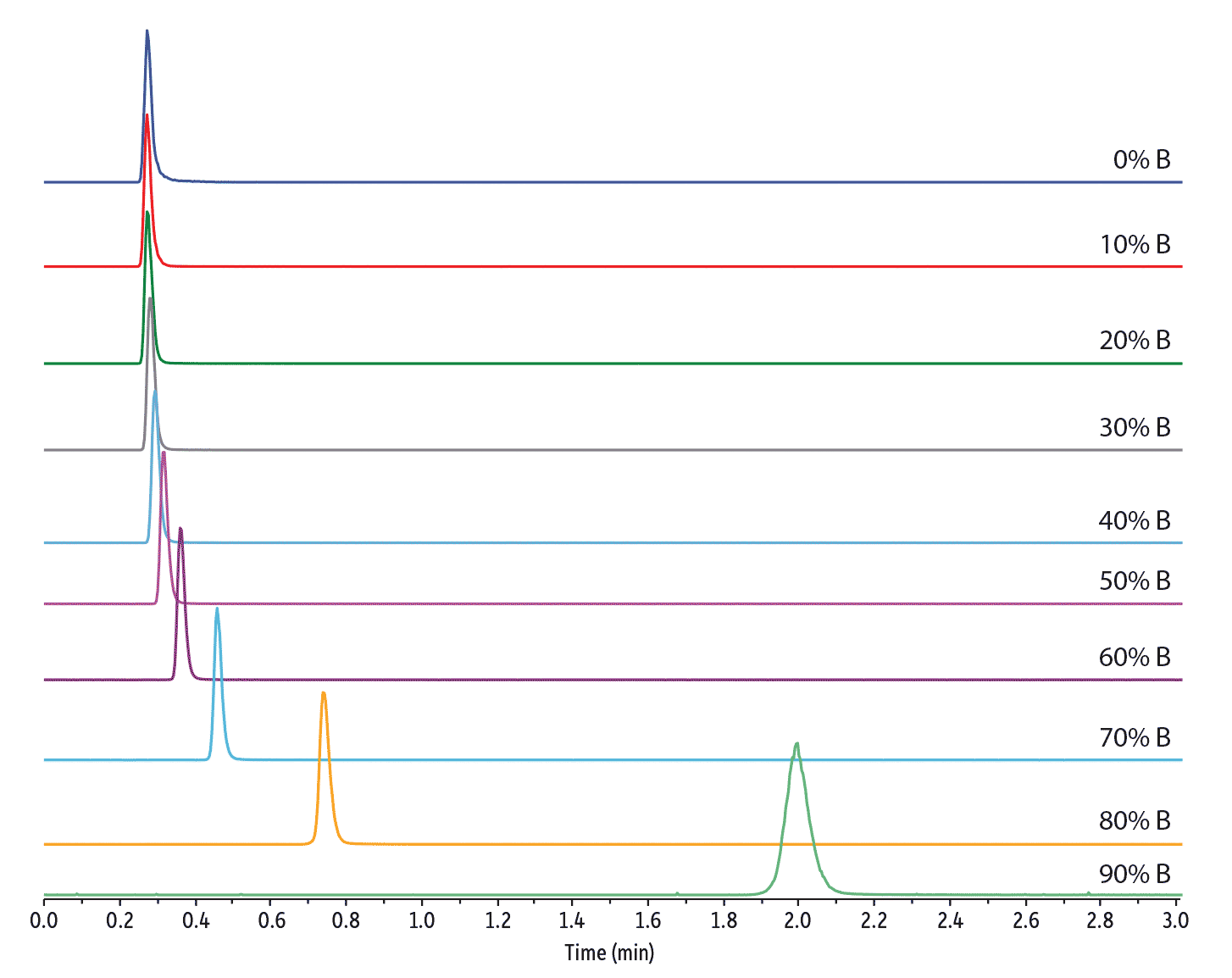
次の例ではFluoroPhenylの陽イオン交換のメカニズムと低分子極性化合物の保持におけるその効果を示します。4-Methylimidazole(4-MEI)は食品や飲料でカラメル色素として用いられる添加物です。他の極性低分子化合物と同様に、非極性固定相での保持が限られているため、標準的な逆相クロマトグラフィーとC18カラムを用いた分析は困難です。しかし、酸性溶液中において4-MEIは正電荷を帯びるため陽イオン交換に非常に適しており 、HILIC条件下で容易に FluoroPhenylへ保持されます。これは5つのフッ素原子の電子求引性で固定相がわずかに負に荷電するためです。図4に示すように、移動相中のアセトニトリル比率が高いとき、陽イオン交換作用が優位になり4-MEIは非常に良く保持されます。逆相条件下において、FluoroPhenyl の保持は分散力が優位になり、4-MEIはほとんど保持されません。FluoroPhenyl固定相は逆相とHILICの両モードで分離性能を評価するという自由度があり、目的化合物に対してどちらが最も効果的かを確認したうえでメソッドを開発・決定することができます。
図 4: 4-MEI のような低分子極性化合物は FluoroPhenyl カラムにおける逆相条件では保持は困難ですが、HILIC条件では容易に保持されます。
| Peaks | |
|---|---|
| 1. | 4-Methylimidazole (4-MEI) |
| Column | Raptor FluoroPhenyl (cat.# 9319A52) |
|---|---|
| Dimensions: | 50 mm x 2.1 mm ID |
| Particle Size: | 2.7 µm |
| Temp.: | 35 °C |
| Standard/Sample | |
| Diluent: | Acetonitrile |
| Conc.: | 100 ng/mL |
| Inj. Vol.: | 5 µL |
| Mobile Phase | Water, 0.1% formic acid:acetonitrile, 0.1% formic acid |
| Flow: | 0.6 mL/min |
| Detector | MS/MS |
|---|---|
| Ion Mode: | ESI+ |
| Mode: | MRM |
| Instrument | UPLC |
移動相条件変更による保持と選択性の微調整
前述の通り、効果的なメソッド開発は慎重なカラム選定にかかっています。そしてFluoroPhenyl固定相では複合的な保持モードにより単一の保持モードしか持たないC18カラムよりも大きな自由度が得られます。この項では移動相組成や酸の強度、酸濃度を変更することで分離を最適化する方法を検討しました。この実験ではFluoroPhenylの多様な保持挙動を実証するためにいくつかの一般的な薬物を選定しました(図5)。これらのテスト化合物は塩基性化合物、弱酸性化合物、中性化合物であり、親水性および塩基性化合物に対する FluoroPhenyl の選択性と親和性の違いを明らかにします。
図 5: Raptor FluoroPhenyl カラムの複数の保持モードを実証するために用いたテスト化合物
移動相組成の影響
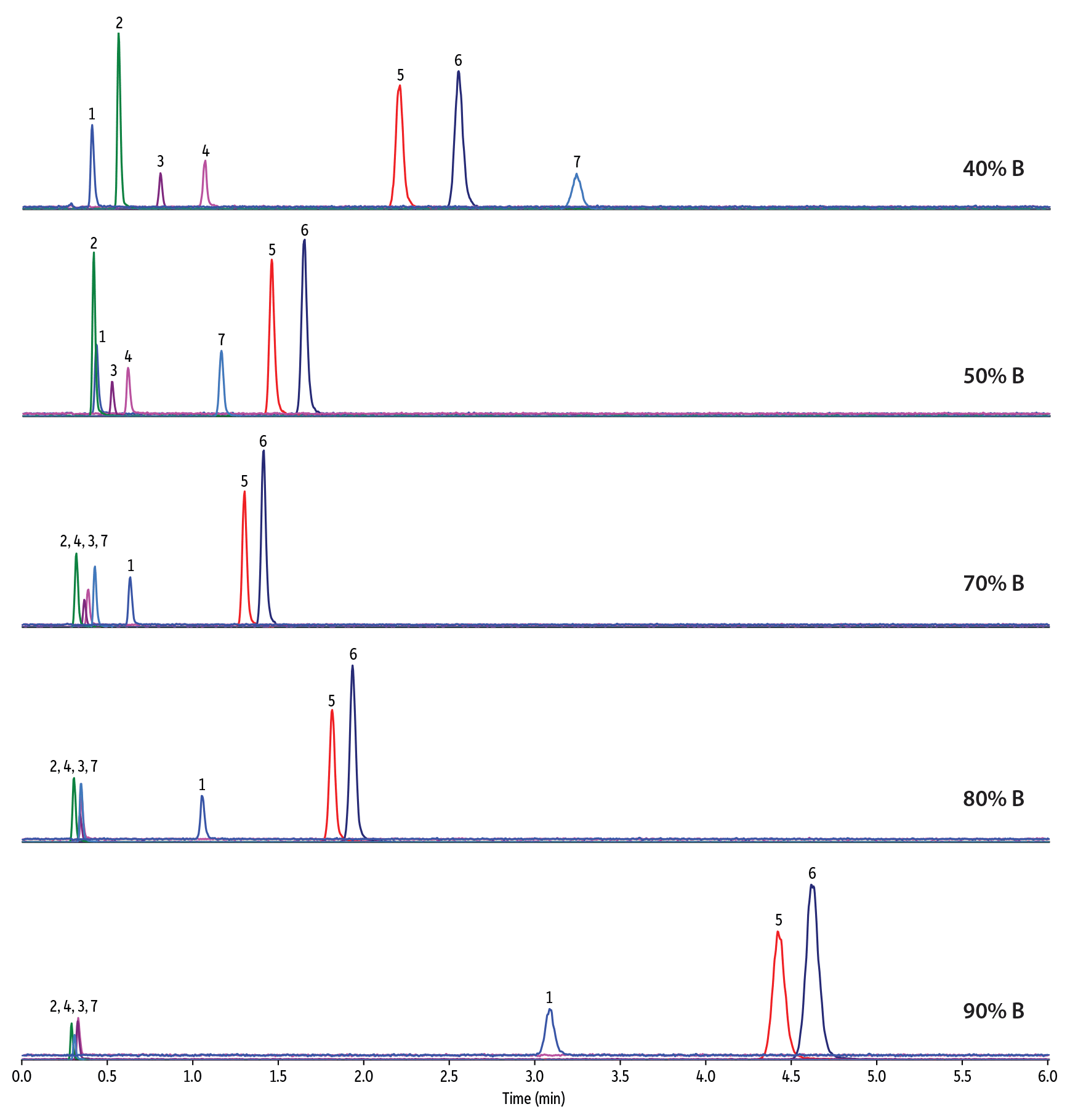
メソッド開発においてFluoroPhenylカラムを選択する主な利点の1つは、HILICと逆相の両モードで使用できることです。移動相組成を変えることで、保持と選択性に変化が起こります。逆相条件下では、分析対象物は分散と極性の相互作用によってFluoroPhenylに保持されます。しかしながら、 移動相中の有機溶媒比率が徐々に高くなるにつれて、 陽イオン交換での保持が優位になることでFluoroPhenyl固定相は正電荷をもつ塩基性化合物を特異的に保持するようになり、中性化合物と酸性化合物はカラムボイド付近に溶出します(図6)。複数の保持機構が作用するFluoroPhenylの実力は、移動相組成を水の比率が高い組成(逆相)から有機溶媒の比率が高い組成(HILIC)へ変更していくにつれ、一部の塩基性化合物で観察される「U字型」の保持挙動によって明確に実証されます。
保持力と選択性に影響を与えるだけでなく、エレクトロスプレーイオン化質量分析(ESI-MS)を使用する場合、有機溶媒比率が高いHILIC移動相へ変更すると、脱溶媒和効率が向上し、感度に大きな影響を与えます。表Iは図6で分析した塩基性化合物のピーク強度を比較したもので、感度増加がノルトリプチリンとアミトリプチリンの両方で観察されたことを示しています。(逆相モードでは保持されなかった化合物がHILICモードで保持されるようになったためであり、アテノロールの感度は変わっていません。)
図 6: 移動相組成を逆相 (40% B) からHILIC (90% B) 条件に変更すると、保持と選択性の変化を示すU字型の保持挙動が得られます。これは固定相に複数の保持メカニズムが存在するために生じます。
| Peaks | Precursor Ion | Product Ion | |
|---|---|---|---|
| 1. | Atenolol | 267.3 | 145.1 |
| 2. | Phenytoin | 253.0 | 181.7 |
| 3. | Trenbolone | 271.2 | 199.2 |
| 4. | Testosterone | 289.2 | 109.1 |
| 5. | Nortriptyline | 264.1 | 91.1 |
| 6. | Amitriptyline | 278.1 | 202.1 |
| 7. | Celecoxib | 382.2 | 362.0 |
| Column | Raptor FluoroPhenyl (cat.# 9319A12) | ||||||
|---|---|---|---|---|---|---|---|
| Dimensions: | 100 mm x 2.1 mm ID | ||||||
| Particle Size: | 2.7 µm | ||||||
| Pore Size: | 90 Å | ||||||
| Temp.: | 40 °C | ||||||
| Standard/Sample | Custom mix | ||||||
| Conc.: | 50 ng/mL (150 ng/mL for phenytoin) | ||||||
| Inj. Vol.: | 1 µL | ||||||
| Mobile Phase | |||||||
| A: | Water + 0.1% formic acid | ||||||
| B: | Acetonitrile + 0.1% formic acid | ||||||
| |||||||
| Max Pressure: | 400 bar |
| Detector | MS/MS |
|---|---|
| Ion Mode: | ESI+ |
| Mode: | MRM |
| Instrument | UHPLC |
表 I: 有機溶媒比率の高い HILIC移動相とESI-MSの組み合わせるによる大幅な感度向上
| Analyte | RP Intensity (40% B, Isocratic) | HILIC Intensity (90% B, Isocratic) | Increase in Response |
|---|---|---|---|
| Atenolol | 5.0e4 | 5.0e4 | – |
| Nortriptyline | 7.5e4 | 1.3e5 | 73% |
| Amitriptyline | 8.5e4 | 1.7e5 | 100% |
移動相中の酸の強度と濃度の影響
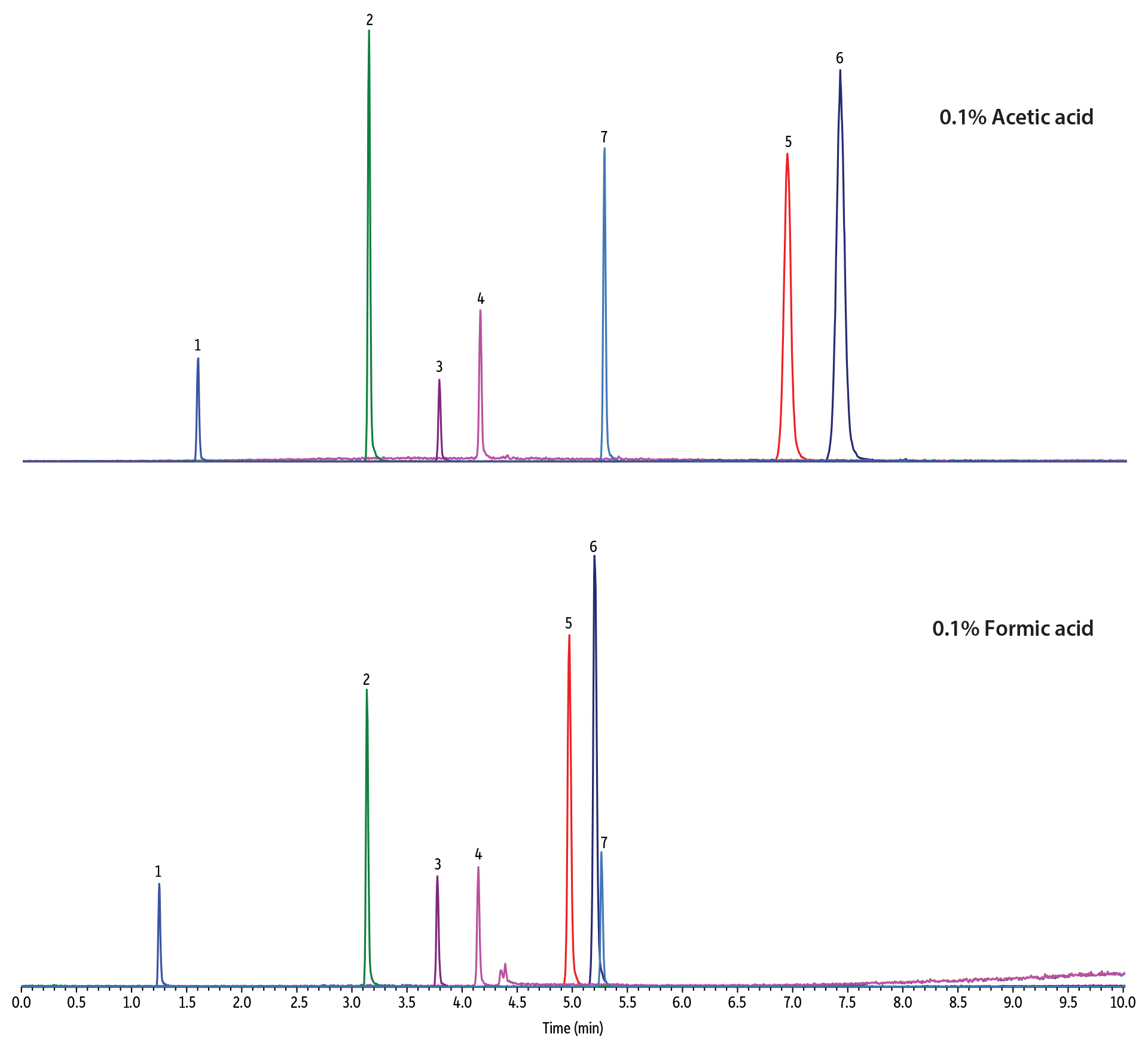
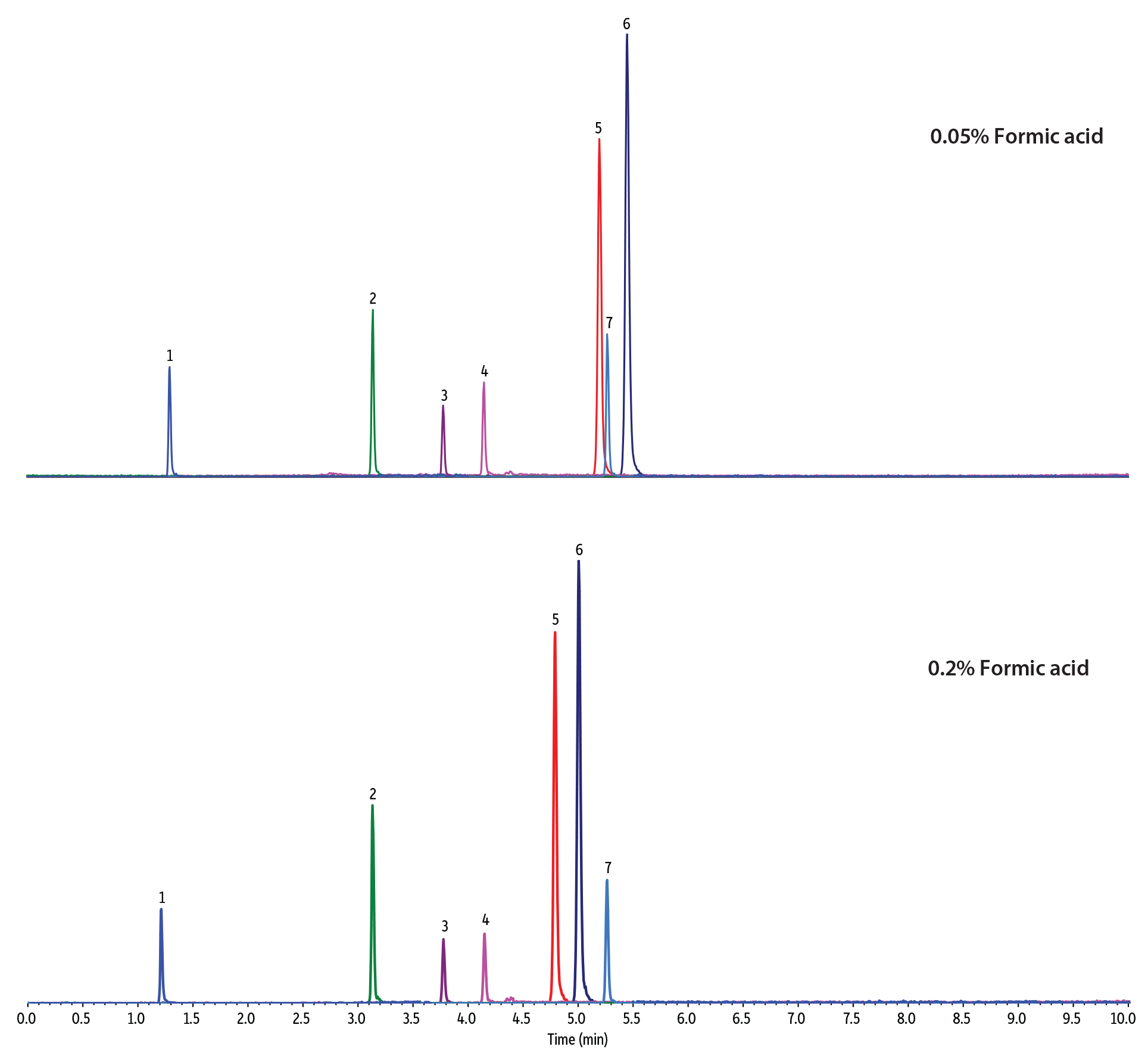
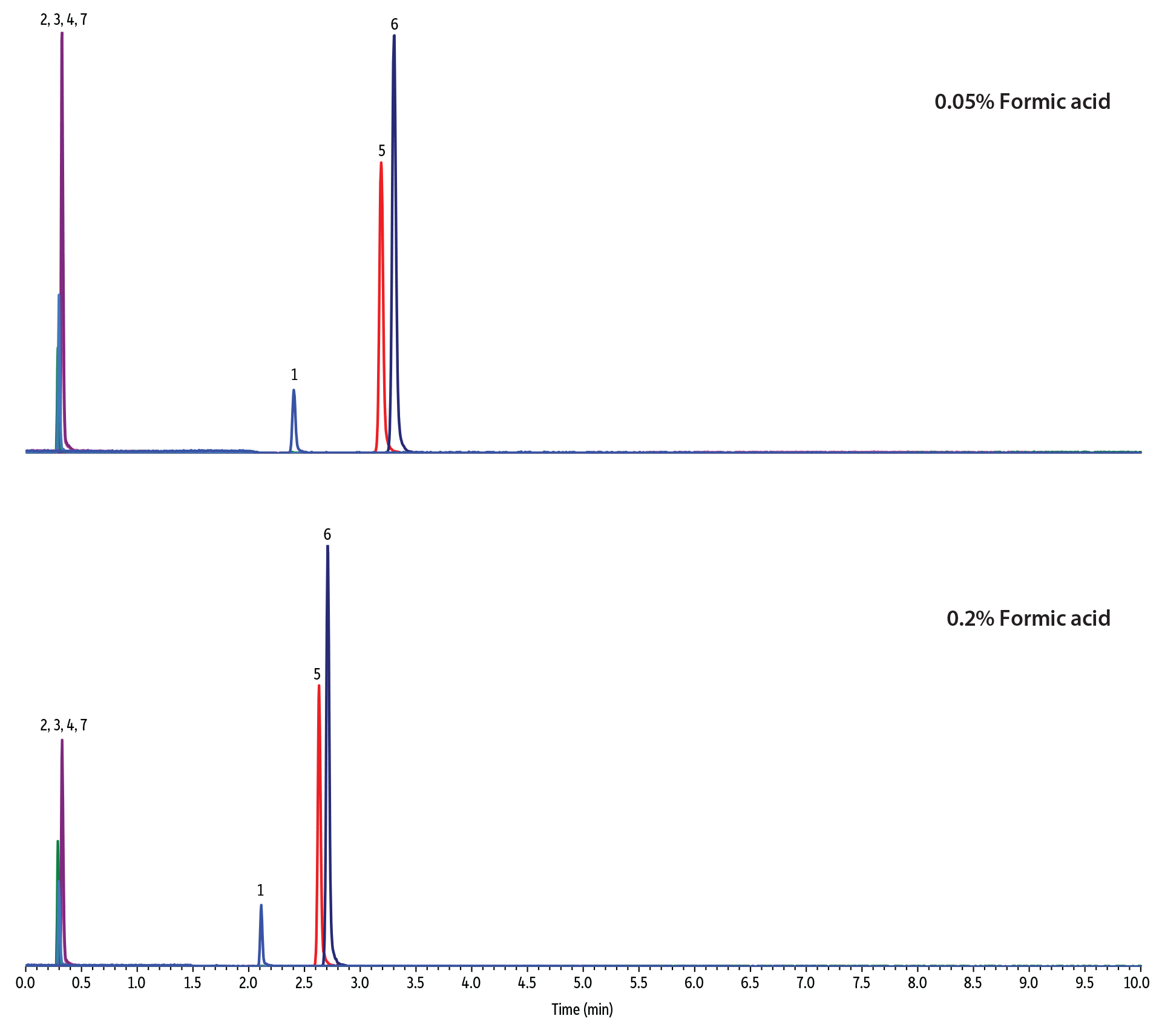
上述のように、移動相の水と有機溶媒の比率を加減することはFluoroPhenylの保持と選択性に著しい変化をもたらし、メソッド開発で特定の分離の最適化をおこないたい場合に、価値のある手段を提供します。さらに、酸性移動相では酸の濃度だけではなく強度もカチオン交換の保持メカニズムに作用し、分離に影響を与える可能性があります。図7に示すように、ギ酸など強酸を含む移動相を用いると、酢酸などより弱酸を同じ濃度で使用した同条件の分析と比較して、塩基性化合物の保持が減少します。しかし、どちらの場合も中性と弱酸性化合物の保持にはほとんど変化がありません。同様に、使用する酸の濃度もFluoroPhenylのカチオン交換保持メカニズムに影響を与える可能性があります。この場合、より高い酸濃度の移動相を使用すると、逆相モードと HILICモードの両方で、中性化合物および弱酸性化合物の保持の変化を最小限に抑えながら、塩基性化合物の保持を減らすことができます(図8)。
図 7:逆相モードにおけるFluoroPhenylの保持と選択性に対する酸強度の影響
| Peaks | Precursor Ion | Product Ion | |
|---|---|---|---|
| 1. | Atenolol | 267.3 | 145.1 |
| 2. | Phenytoin | 253.0 | 181.7 |
| 3. | Trenbolone | 271.2 | 199.2 |
| 4. | Testosterone | 289.2 | 109.1 |
| 5. | Nortriptyline | 264.1 | 91.1 |
| 6. | Amitriptyline | 278.1 | 202.1 |
| 7. | Celecoxib | 382.2 | 362.0 |
| Column | Raptor FluoroPhenyl (cat.# 9319A12) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Dimensions: | 100 mm x 2.1 mm ID | ||||||||||||||||||||
| Particle Size: | 2.7 µm | ||||||||||||||||||||
| Pore Size: | 90 Å | ||||||||||||||||||||
| Temp.: | 40 °C | ||||||||||||||||||||
| Standard/Sample | Custom mix | ||||||||||||||||||||
| Diluent: | Water | ||||||||||||||||||||
| Conc.: | 50 ng/mL (150 ng/mL for phenytoin) | ||||||||||||||||||||
| Inj. Vol.: | 1 µL | ||||||||||||||||||||
| Mobile Phase | |||||||||||||||||||||
| A: | Water + 0.1% acid | ||||||||||||||||||||
| B: | Acetonitrile + 0.1% acid | ||||||||||||||||||||
| |||||||||||||||||||||
| Max Pressure: | 400 bar |
| Detector | MS/MS |
|---|---|
| Ion Mode: | ESI+ |
| Mode: | MRM |
| Instrument | UHPLC |
図 8: FluoroPhenylの保持と選択性に対する酸強度の影響
Reversed-Phase Mode
| Peaks | Precursor Ion | Product Ion | |
|---|---|---|---|
| 1. | Atenolol | 267.3 | 145.1 |
| 2. | Phenytoin | 253.0 | 181.7 |
| 3. | Trenbolone | 271.2 | 199.2 |
| 4. | Testosterone | 289.2 | 109.1 |
| 5. | Nortriptyline | 264.1 | 91.1 |
| 6. | Amitriptyline | 278.1 | 202.1 |
| 7. | Celecoxib | 382.2 | 362.0 |
| Column | Raptor FluoroPhenyl (cat.# 9319A12) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Dimensions: | 100 mm x 2.1 mm ID | ||||||||||||||||||||
| Particle Size: | 2.7 µm | ||||||||||||||||||||
| Pore Size: | 90 Å | ||||||||||||||||||||
| Temp.: | 40 °C | ||||||||||||||||||||
| Standard/Sample | Custom mix | ||||||||||||||||||||
| Diluent: | Water | ||||||||||||||||||||
| Conc.: | 50 ng/mL (150 ng/mL for phenytoin) | ||||||||||||||||||||
| Inj. Vol.: | 1 µL | ||||||||||||||||||||
| Mobile Phase | |||||||||||||||||||||
| A: | Water + x% formic acid | ||||||||||||||||||||
| B: | Acetonitrile + x% formic acid | ||||||||||||||||||||
| |||||||||||||||||||||
| Max Pressure: | 400 bar |
| Detector | MS/MS |
|---|---|
| Ion Mode: | ESI+ |
| Mode: | MRM |
| Instrument | UHPLC |
HILIC Mode
| Peaks | Precursor Ion | Product Ion | |
|---|---|---|---|
| 1. | Atenolol | 267.3 | 145.1 |
| 2. | Phenytoin | 253.0 | 181.7 |
| 3. | Trenbolone | 271.2 | 199.2 |
| 4. | Testosterone | 289.2 | 109.1 |
| 5. | Nortriptyline | 264.1 | 91.1 |
| 6. | Amitriptyline | 278.1 | 202.1 |
| 7. | Celecoxib | 382.2 | 362.0 |
| Column | Raptor FluoroPhenyl (cat.# 9319A12) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Dimensions: | 100 mm x 2.1 mm ID | ||||||||||||||||||||
| Particle Size: | 2.7 µm | ||||||||||||||||||||
| Pore Size: | 90 Å | ||||||||||||||||||||
| Temp.: | 40 °C | ||||||||||||||||||||
| Standard/Sample | Custom mix | ||||||||||||||||||||
| Diluent: | Methanol | ||||||||||||||||||||
| Conc.: | 50 ng/mL (150 ng/mL for phenytoin) | ||||||||||||||||||||
| Inj. Vol.: | 1 µL | ||||||||||||||||||||
| Mobile Phase | |||||||||||||||||||||
| A: | Water, x% formic acid | ||||||||||||||||||||
| B: | Acetonitrile, x% formic acid | ||||||||||||||||||||
| |||||||||||||||||||||
| Max Pressure: | 400 bar |
| Detector | MS/MS |
|---|---|
| Ion Mode: | ESI+ |
| Mode: | MRM |
| Instrument | UHPLC |
まとめ
メソッド開発が成功するかどうかは、カラム選択が大きな鍵となります。C18カラムが第一選択である一方で、分析対象物の化学的性質を固定相の特性とともに慎重に検討する必要があります。なぜなら、FluoroPhenyl固定相は複数の保持メカニズム(分散、立体選択性、陽イオン交換、双極子、およびπ-π)を有するため、主に分散作用しか利用しないC18と比較してFluoroPhenyは異なる選択性を提供するからです。ここで示したように、逆相と HILICモードの両方で使用できる FluoroPhenylの複数の保持メカニズムは、C18では達成できない分離を成し遂げます。さらに、移動相組成、酸の強度、ならびに酸濃度を変更することで分離をさらに向上することができ、より多くの保持と選択性が利用可能となります。

